Die Angstmacher
Neue Gesetze töten Menschen - solche Behauptungen sollen Politiker an der kurzen Leine der Industrie halten. Und die schwärmt von guten Zugängen in die Politik.
Florence leidet. Im Morgenmantel schleppt sich die ältere blonde Frau durch den Flur eines Krankenhauses. Dann setzt sie sich und schaut mit leeren Augen in die Kamera. Florence braucht eine lebensrettende Operation. Aus dem Off sagt eine Stimme, dass ein neues EU-Gesetz - die sogenannte Medizinprodukteverordnung - in Europa dazu führen würde, dass Florence drei Jahre auf den Eingriff warten müsste. Diese Zeit habe sie nicht, ist auf dem Bildschirm zu lesen. Kurzum: Florence müsste wegen der Brüsseler Bürokraten sterben.
So zumindest geht die Geschichte in diesem Videoclip von 2013.
In Wahrheit ist Florence gar nicht krank, sie ist Schauspielerin und ihr leidender Auftritt Teil einer professionellen Medienkampagne. Das Ziel: Es soll so einfach bleiben wie bisher, Herzschrittmacher, Knieprothesen oder Insulinpumpen auf den Markt zu bringen. Bloß keine strengeren Regeln, bloß keine aufwendigen Studien.
Ein Film suggeriert, dass Menschen wegen verschärfter Gesetze sterben würden: Selbst hartgesottene EU-Parlamentarier bezeichnen die Lobbykampagne, die der europäische Verband Eucomed in den Jahren 2012 und 2013 führte, als beispiellos.

imago
"Ich war 25 Jahre in Brüssel, aber einen solchen Lobbydruck hatte ich noch nie erlebt", sagt Dagmar Roth-Behrendt, die von 1989 bis 2014 für die SPD im EU-Parlament saß.
Als sogenannte Berichterstatterin sollte sie die Warum die neue EU-Richtlinie Ärzte und Patientenvertreter enttäuschtneue EU-Verordnung zur Zertifizierung von MedizinproduktenWarum die neue EU-Richtlinie Ärzte und Patientenvertreter enttäuscht mitschreiben. Neben dem Video seien Zeitungsanzeigen geschaltet und die EU-Parlamentarier "intensivst bearbeitet" worden. "Das war unterste Schublade, echt widerlich", sagt Roth-Behrendt.
Unbestritten ist, dass Medizinprodukte jedes Jahr die Leben von Millionen Menschen verlängern oder retten. Gleichzeitig stand Europa in den vergangenen Jahren im Zentrum einiger der schlimmsten Medizinprodukt-Skandale. Zum Beispiel bekamen Frauen zwischen 1995 und 1999 Brustimplante mit einer gesundheitsschädlichen Füllung aus Sojaöl. So etwas kann in Europa besonders leicht passieren, weil das Zertifizierungssystem für Medizinprodukte hier ist, wie es ist: privatisiert und unzuverlässig.
Anders als Medikamente müssen Implantate und Prothesen nicht darauf getestet werden, ob sie Patienten wirklich helfen, sondern ob sie technisch funktionieren. Nicht staatliche Stellen entscheiden, was implantiert werden darf. Stattdessen zertifizieren private Unternehmen wie TÜV oder die Dekra die Geräte. Dabei prüfen sie meist nur die technischen Unterlagen, aber nicht die Geräte selbst. Diese Firmen verdienen aber nur dann Geld, wenn sie einen Prüfauftrag von den Herstellern bekommen.
Deshalb bringen viele Unternehmen ihre Produkte zuerst in Europa auf den Markt, bevor sie es in den USA versuchen, wo die Regeln viel strenger sind. So war es etwa bei Pleuraseal, einem Lungen-Dichtmittel, das zum Beispiel bei Operationen verhindern sollte, dass Luft aus der Lunge in das umliegende Gewebe entweicht, aber doch nicht so gut abdichtete wie geplant. Und so war es auch bei Robodoc, einem Operationsroboter des Herstellers Integrated Surgical Systems (ISS), der zahlreiche Menschen verletzte. Eine Anfrage ließ der Hersteller unbeantwortet.
In Europa seien Patienten die "Versuchskaninchen", kritisierte im Jahr 2011 Jeffrey Shuren von der US-Aufsichtsbehörde FDA.
Medizinprodukte sind ein Milliardengeschäft. In der Bundesrepublik forschen und fertigen mehr als 12.000 Unternehmen, die Palette reicht vom einfachen Holzspatel bis hin zur aufwendigen Wirbelsäulenprothese. Gleich vier Lobbyverbände kümmern sich um die Interessen der Branche: die Zentralvereinigung medizin-technischer Fachhändler, Hersteller, Dienstleister und Berater, der Verband der Diagnostica-Industrie, der Medizintechnikverband Spectaris und nicht zuletzt der BVMed, der größte und einflussreichste Interessenvertreter. Drei davon sind Mitglieder im europäischen Dachverband MedTech Europe – und der hat vor allem ein Ziel: Alles soll so bleiben, wie es ist.
Die EU-Kommission hingegen wollte bereits 2008 den Wandel. Nie mehr sollten fehlerhafte Implantate ungeprüft eingesetzt werden. Nie mehr sollten auslaufende Brustimplantate Tausenden Frauen schaden, nie wieder defekte Herzschrittmacher an Menschen tödliche Stromstöße abgeben. Wie in den USA sollten Produkte systematisch auf ihren klinischen Nutzen getestet werden, eine staatliche Behörde sollte alles überwachen. Besonders risikobehaftete Produkte sollten von staatlicher Seite getestet werden, nicht mehr von Privatunternehmen.
Ärzteverbände, Verbraucherschützer und Patientenorganisationen waren angesichts des EU-Vorstoßes im Jahr 2008 voller Hoffnung. MedTech Europe dagegen war empört. „Das Wohl der Patienten und der Zugang zu neuer Medizintechnologie wird in unseren Augen wahrscheinlich darunter leiden", warnten die Lobbyisten die EU-Kommission. Die Vorschläge seien alarmierend und „total inakzeptabel“.
Die Lobbyisten klangen, als stehe der Untergang des Patientenwohls bevor. Vom Brüsseler Bürokratiemonster war die Rede, von Regularien, die mittelständische Unternehmen in den Ruin treiben und Fortschritt verhindern würden. Die Lobbyisten schwärmten aus.
Als der damalige EU-Gesundheitskommissar John Dalli vier Jahre später, im Februar 2012, vor die Presse trat, um eine „Verbesserung der Patientensicherheit“ zu fordern, konnte man bereits eine erste Abschwächung seiner früheren Aussagen heraushören. Hatte es beispielsweise früher noch geheißen, das bestehende Zulassungssystem sei „unzureichend“, hieß es nun, dass die Regularien keinesfalls „grundsätzlich unzuverlässig“ seien. Die offensichtlichen Gründe für die neue Milde waren zwischen den Zeilen zu hören: So habe es "gezielte Treffen mit hochrangigen Vertretern der Industrieverbände und Benannten Stellen" gegeben, wie es in einem Arbeitspapier der EU-Kommission vom September 2012 heißt. Benannte Stellen, das sind die privaten Prüfunternehmen. Wer wen wann genau getroffen hatte, wurde in dem Dokument nicht offengelegt.
Dasselbe Arbeitspapier stellte fest, dass Medizinprodukte in Europa schneller auf den Markt kämen als in den USA, "während die Sicherheitsstandards als gleich angesehen werden". Die Studie, auf die sich die Kommission in diesem Zusammenhang bezog, stammte von der Beratungsfirma Boston Consulting Group - deren Arbeit von allerlei Lobbyisten aus den USA finanziert wurde.

"Mir war es wichtig, dass nicht nur Arzneimittel sicher sind, sondern dass auch Medizinprodukte sicher sind", erklärt die ehemalige EU-Parlamentarierin Dagmar Roth-Behrendt, 65, im Interview mit SZ, NDR und WDR. 500 Millionen Menschen leben in der Europäischen Union, sie alle könnten von strengeren Regeln profitieren. Implantate, die besser getestet sind, verheißen weniger Komplikationen, geringere Kosten für Versicherungen, am Ende gar geringere Beiträge für die Versicherten. Oder ganz einfach: ein längeres und besseres Leben.
Für Hersteller bedeuten strengere Regeln indes Kosten und längere Fristen, bis ein Produkt auf den Mark kommt. Die privaten Prüfer verlören durch staatliche Kontrolle ein Geschäftsmodell. Spürbar war diese Furcht wieder im Sommer dieses Jahres, als sich mehrere Dutzend Firmenvertreter in der Stadthalle von Tuttlingen trafen. Vermutlich in keinem anderen Teil Deutschlands sitzen so viele Medizinproduktehersteller wie im baden-württembergischen Wahlkreis von Volker Kauder (CDU), bis September dieses Jahres Vorsitzender der Unionsfraktion im Bundestag und treuer Gefährte Angela Merkels.
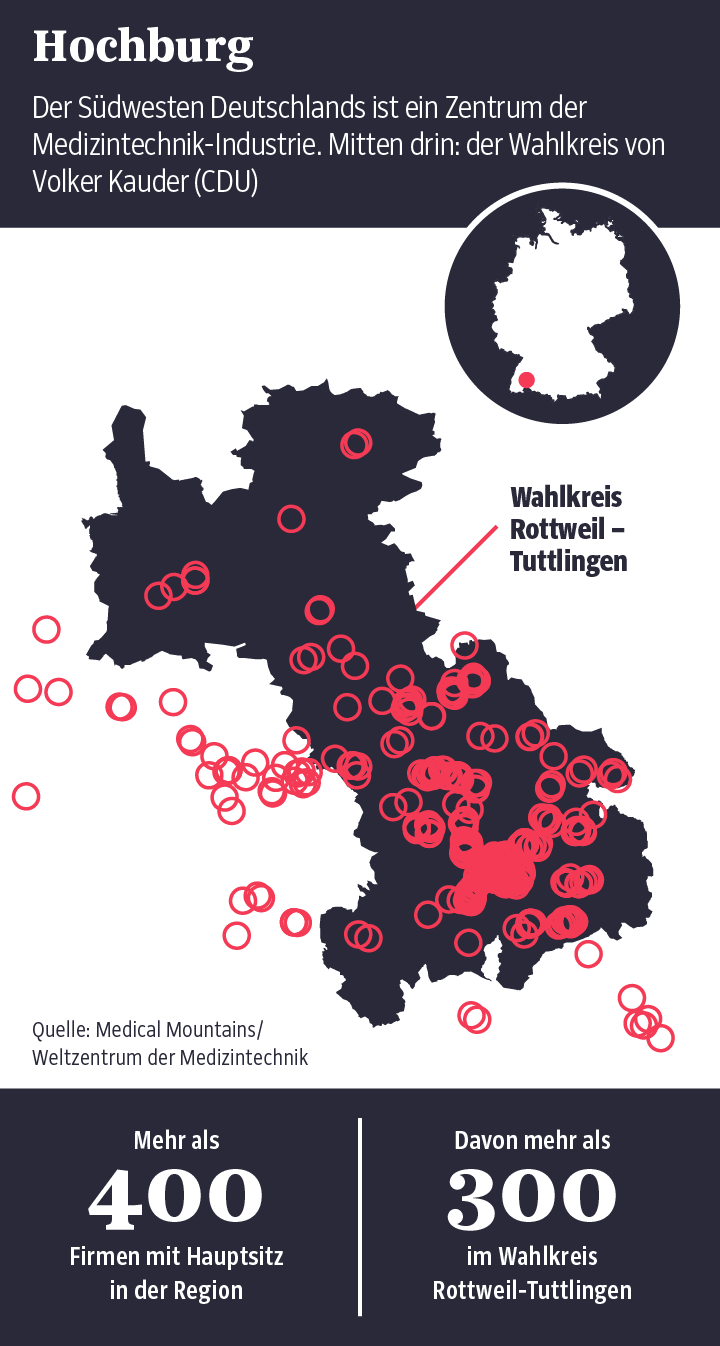
„Medical Mountains“ nennt sich der Zusammenschluss der Tuttlinger Medizinproduktfirmen. Sie sind geübt darin, ihren Einfluss geltend zu machen. Martin Leonhard etwa arbeitet für den Endoskopehersteller Karl Storz und ist gleichzeitig Vorsitzender des Bereichs Medizintechnik beim Lobbyverband Spectaris. „Seit dem Entwurf der Medizinprodukte-Verordnung 2012 bin ich in der politischen Diskussion sehr aktiv gewesen und habe die Unternehmens- und Verbandsinteressen in Brüssel, Berlin und Stuttgart vertreten“, berichtet Leonhard den Kollegen in der Stadthalle von Tuttlingen.

Pressematerial Storz/Bildbearbeitung von SZ
In der heißen Phase der EU-Gesetzgebung hat Leonhard nicht nur Volker Kauder mit Firmenvertretern aus dessen Heimat zusammengeführt, sondern auch Jens Spahn, den damaligen gesundheitspolitischen Sprecher der Unionsfraktion im Bundestag und heutigen Gesundheitsminister, sowie Annette Widmann-Mauz (beide CDU), bis März 2018 Staatssekretärin im Gesundheitsministerium, nach Tuttlingen geholt. Leonhard verkündete, was man erreicht habe in den fünf Jahren Diskussion über die Medizinprodukteverordnung: "Es gibt keine zentrale europäische Zulassungsstelle. Es gibt auch keine Nutzenbewertung."
Leicht sei das nicht gewesen, denn "die Frau Roth-Behrendt" - die Berichterstatterin der SPD - "hat sich sehr massiv eingesetzt für strengere Regeln“. Ein Problem sei auch gewesen, dass viele europäische Länder politisch "vor allem die Patienten vertreten".
Volker Kauder weiß, was Medizinproduktehersteller brauchen. So soll er sich auf europäischer Ebene für den Erhalt einer Sonderregel eingesetzt haben, durch die sich Unternehmen bei Skalpellen und anderem, weniger riskantem chirugischem Besteck das CE-Kennzeichen quasi selbst erteilen können. Solche Firmen also, von denen besonders viele in Kauders Wahlkreis ansässig sind. Eine Art "Lex Tuttlingen". In einer Stellungnahme aus dem Gesundheitsministerium von 2014, die SZ, WDR und NDR einsehen konnten, heißt es: „Auch Herr MdB Dr. Kauder hatte sich in dieser Angelegenheit bereits an Herrn Minister gewandt.“ Gemeint ist der damalige Gesundheitsminister und CDU-Parteifreund Hermann Gröhe. Im März 2016 schreibt eine Referatsleiterin in einer E-Mail, dass sich das Ministerium dafür einsetzen werde, dass OP-Besteck weiterhin nicht von einer Prüfbehörde zertifiziert werde - "nicht zuletzt aufgrund der Interventionen von MdB Kauder". Auf Anfrage wollte sich Kauder nicht äußern.
Gemeint ist der damalige Gesundheitsminister und CDU-Parteifreund Hermann Gröhe. Im März 2016 schreibt eine Referatsleiterin in einer E-Mail, dass sich das Ministerium dafür einsetzen werde, dass OP-Besteck weiterhin nicht von einer Prüfbehörde zertifiziert werde - "nicht zuletzt aufgrund der Interventionen von MdB Kauder". Auf Anfrage wollte sich Kauder nicht äußern.
Wer mit Vertretern der deutschen MedTech-Europe-Mitglieder BVMed und Spectaris spricht, hört vor allem eines: wie gut die Zugänge in die Politik im Allgemeinen und in das Gesundheitsministerium im Speziellen seien. Mehrmals pro Woche gebe es Gespräche, der Minister und seine Staatssekretäre hätten stets ein offenes Ohr.
Kritische Stimmen wie der ehemalige Chef des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM), Harald Schweim, drücken es so aus:
Die Lobby habe die Politiker "auf Pfiff bei Fuß. Besser als meine Hunde parieren".
Tatsächlich deckt sich dies mit den Erkenntnissen aus Hunderten Seiten bislang vertraulicher Unterlagen des Gesundheitsministeriums, die SZ, NDR und WDR ausgewertet haben. Sie zeichnen das Bild eines Ministeriums, das Argumente der Industrie teils ungeprüft übernimmt und das Wohl der Patienten gelegentlich aus den Augen zu verlieren scheint. Ein Beispiel: Als diskutiert wurde, ob Hersteller künftig nachweisen sollten, dass ihr Produkt einen medizinischen Nutzen bringe, hieß es in einer internen E-Mail aus einem Referat des Gesundheitsministeriums vom 16. November 2011: "Dies ist aber in keinem Markt der Welt derzeit gefordert und würde mit diesem totalitären Anspruch gegen elementare Grundsätze der freien Marktwirtschaft oder des Wettbewerbs stehen."
Parallel dazu kam die gespielte Kranke Florence zum Einsatz. 277 Tage nachdem ihr Video online ging, stimmte das EU-Parlament im Oktober 2013 für eine entschärfte Version der Verordnung - ohne staatliche Zulassungsbehörde und ohne die Verpflichtung, Medizinprodukte auf ihren Nutzen für Patienten zu testen. Dagmar Roth-Behrendt, die Verfechterin von strengeren Regeln, hatte verloren. „Das macht mich so wütend, dass ich auch anfangen kann zu weinen“, sagt sie heute.
Zu einem Systemwandel kam es trotz mehrjähriger Verhandlungen also nicht: Statt einer staatlichen Behörde entscheiden weiterhin Privatunternehmen über die Zulassung neuer Medizinprodukte. Ob ein Gerät Patienten wirklich nützt, muss ebenfalls nicht vorher geprüft werden. Dafür müssen die sogenannten Benannten Stellen nun unangemeldet bei den Herstellern kontrollieren - mindestens einmal alle fünf Jahre. Bisher gab es keine solch verbindliche Anweisung.
Für MedTech Europe war das ein Grund zum Feiern. Auf einer Konferenz jubelte ein MedTech-Europe-Vertreter im Herbst 2017, dass "große Innovationshemmnisse" entfernt oder ausgeglichen" worden seien: Eine öffentliche Zulassungsbehörde wie in den USA? Tests zum klinischen Nutzen? Gebe es nicht.
Florence, die Frau aus dem Werbespot, kann sich also freuen. Zwar hat sich inzwischen herausgestellt, dass ihre gewünschte Wunderbehandlung nun doch nicht so viel Erfolg verspricht. Eines aber hat die Kampagne immerhin bewirkt: Sie hat den Staat als Beschützer der Patienten auf Abstand gehalten.

Das sind die Implant Files
Implantate können Leben retten - oder zerstören. Über einen Medizin-Skandal, der sich Tag für Tag wiederholt.